다음 Arrhenius식에 대한 설명으로 옳지 않은 것은?
문제풀이 모드
0
정답률 : -
다음 Arrhenius식에 대한 설명으로 옳지 않은 것은?
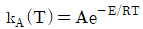
A는 지수 앞자리인자 또는 빈도인자이다.
활성화에너지의 단위는 J/mol 또는 cal/mol이다.
e-E/RT는 반응이 일어나기에 충분한 최소에너지 E를 가지는 분자들 사이의 충돌분율을 나타낸다.
활성화에너지 E는 전환이 된 후 분자들이 가져야 하는 최소에너지이다.
채점하기












